Учёные обнаружили, что бактерии способны «взрываться» ради распространения устойчивости к антибиотикам
Бактерии перестраивают собственную «иммунную систему» таким образом, чтобы разрывать свою оболочку и обмениваться ДНК, — и тем самым подпитывают распространение устойчивости к антибиотикам.
Аннотация:
Учёные выявили неожиданную особенность механизма, с помощью которого бактерии обмениваются генами, — в том числе теми, которые обеспечивают устойчивость к антибиотикам. Мельчайшие вирусоподобные частицы, называемые агентами переноса генов (англ. gene transfer agents, GTA), которые когда-то были древними вирусными захватчиками, со временем были приспособлены бактериями и превращены в системы доставки, переносящие ДНК от одной клетки к другой. В ходе исследования был обнаружен ключевой управляющий узел из трёх генов, получивший обозначение LypABC, который запускает процесс разрыва бактериальных клеток и высвобождения этих «курьеров», нагруженных ДНК.
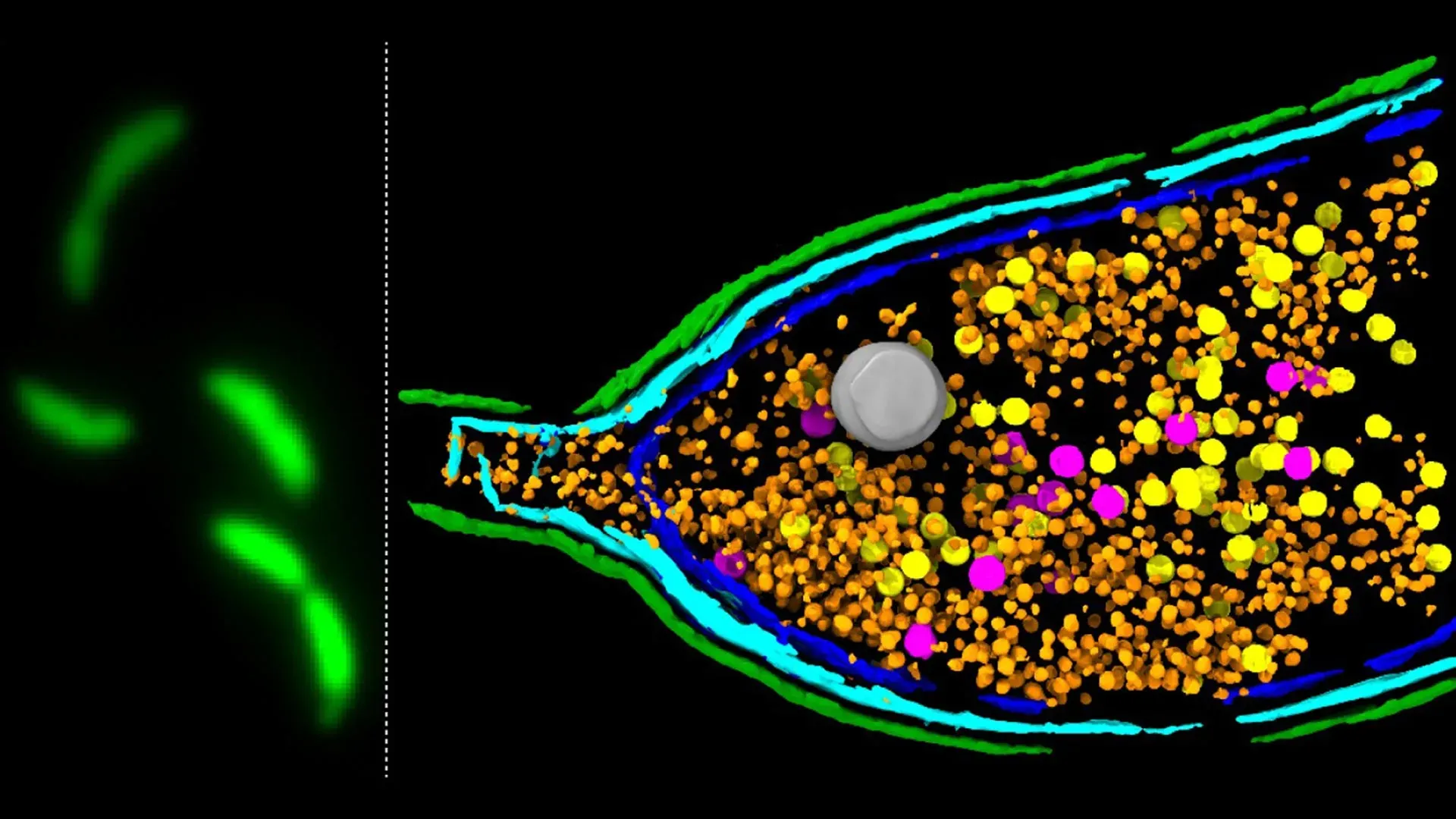
Учёные раскрыли новые подробности того, каким образом бактерии обмениваются генами, — в том числе генами, ответственными за устойчивость к противомикробным препаратам (антимикробную резистентность, АМР), которая представляет собой нарастающую угрозу для мирового здравоохранения. Эти результаты были получены исследователями из Центра Джона Иннеса, изучавшими необычные частицы, известные как агенты переноса генов (GTA).
Агенты переноса генов внешне напоминают бактериофаги — вирусы, поражающие бактерии, — однако давно перестали быть вредоносными захватчиками. По своему происхождению они восходят к древним вирусам, которые бактерии в процессе эволюции приспособили и поставили под собственный контроль.
Вирусоподобные частицы доставляют ДНК от клетки к клетке
Эти частицы работают как миниатюрные транспортные средства. Они подхватывают фрагменты ДНК из одной бактериальной клетки и переносят их к соседним клеткам. Этот процесс, называемый горизонтальным переносом генов, позволяет бактериям быстро обмениваться полезными признаками, в том числе генами, которые помогают им выживать при лечении антибиотиками.
Ключевым этапом этого процесса является лизис клетки-хозяина — разрушение бактериальной клетки, в результате которого частицы GTA высвобождаются наружу. До сих пор учёные не до конца понимали, каким именно образом эти частицы покидают клетку-хозяина.
Ключевой генный кластер управляет лизисом клетки
В исследовании, опубликованном в журнале Nature Microbiology, научная группа применила метод скрининга на основе глубокого секвенирования для точного определения генов, участвующих в работе GTA в модельном организме — бактерии Caulobacter crescentus.
Был выявлен трёхгенный комплекс под названием LypABC, кодирующий бактериальные белки. Когда гены lypABC были удалены, клетки утрачивали способность разрушаться и высвобождать частицы GTA. Когда же этот комплекс был принудительно активирован сверх нормы, значительная часть клеток подвергалась лизису. Эти результаты показывают, что LypABC выполняет роль центрального управляющего узла данного процесса.
Иммунная система, перестроенная для переноса генов
Одним из самых неожиданных открытий стало то, что система LypABC обнаруживает близкое сходство с бактериальной антифаговой иммунной системой. В её составе присутствуют белковые компоненты, которые обычно связаны с защитой от вирусов. Однако в данном случае эта система, по всей видимости, была эволюционно перестроена таким образом, чтобы способствовать высвобождению частиц GTA и содействовать переносу генов.
Данная работа, выполненная совместно с Йоркским университетом и Роулендовским институтом при Гарварде, наглядно демонстрирует, что бактерии способны использовать уже имеющиеся биологические системы совершенно неожиданным образом.
Строгая регуляция необходима для выживания
Кроме того, исследователи обнаружили регуляторный белок, обеспечивающий строгий контроль над активностью GTA. Такая регуляция критически важна, поскольку неконтролируемая активация LypABC может оказаться крайне токсичной для самих бактериальных клеток.
Показав, насколько пластичными могут быть бактериальные системы, данное исследование углубляет наше понимание того, как гены перемещаются от клетки к клетке. Этот процесс играет ключевую роль в распространении устойчивости к антибиотикам.
Новые ключи к пониманию в борьбе с устойчивостью к антибиотикам
Первый автор исследования, д-р Эмма Бэнкс, стипендиат-исследователь Королевской комиссии Всемирной выставки 1851 года, отметила: «Особенно интересно то, что LypABC по своей структуре напоминает иммунную систему, и тем не менее бактерии используют её для высвобождения частиц GTA. Это наводит на мысль о том, что иммунные системы могут быть эволюционно перенастроены таким образом, чтобы помогать бактериям обмениваться ДНК друг с другом, — а это процесс, способствующий распространению устойчивости к антибиотикам».
Следующим шагом станет выяснение того, каким образом система LypABC активируется и как именно она управляет разрывом бактериальных клеток для высвобождения частиц GTA.
Новое исследование пролило важный свет на бывших врагов, ставших союзниками, — на механизм, позволяющий бактериям обмениваться генами, в том числе теми, которые связаны с устойчивостью к противомикробным препаратам (АМР).
Эти открытия, расширяющие наше понимание АМР как одной из главных глобальных угроз здоровью, были сделаны исследователями из Центра Джона Иннеса в ходе изучения любопытного феномена — агентов переноса генов (GTA).
Эти частицы-носители генов внешне похожи на бактериофаги — вирусы, поражающие бактерии, — однако они были «одомашнены» из древних вирусов и поставлены на службу бактериальной клетке-хозяину.
Выступая в роли курьеров, они забирают «посылки» с ДНК клетки-хозяина и доставляют их соседним бактериям. Такой «бескорыстный» обмен, известный как горизонтальный перенос генов, способен стремительно распространять полезные признаки, включая гены, обеспечивающие устойчивость к антибиотикам, применяемым для лечения инфекций.
Важнейшим этапом жизненного цикла GTA является лизис клетки-хозяина — её разрушение с целью высвобождения частиц GTA, нагруженных ДНК. Ранее оставалось неясным, каким образом частицы GTA покидают бактериальную клетку-хозяина.
В данном исследовании, опубликованном в журнале Nature Microbiology, научная группа использовала метод скрининга на основе глубокого секвенирования для выявления генов, критически важных для функционирования GTA в модельной бактерии Caulobacter crescentus.
В результате был обнаружен трёхгенный управляющий узел LypABC, кодирующий бактериальные белки. При удалении генов lypABC бактерии утрачивали способность к лизису и, соответственно, не могли высвобождать частицы GTA. Напротив, при искусственной сверхэкспрессии узла lypABC наблюдалась очень высокая доля клеток, подвергающихся лизису. В совокупности эти эксперименты позволили установить, что LypABC представляет собой механизм управления лизисом клеток, опосредованным GTA.
Неожиданным оказалось то, что LypABC обнаруживает сходство с бактериальной антифаговой иммунной системой, поскольку содержит белковые домены, обычно задействованные в защите от вирусов. Однако результаты этой совместной работы Центра Джона Иннеса, Йоркского университета и Роулендовского института при Гарварде указывают на то, что данная система была эволюционно перенастроена для высвобождения частиц GTA в целях переноса генов.
Кроме того, исследователи выявили регуляторный белок, необходимый для строгого контроля как активации GTA, так и опосредованного ими лизиса. Этот контроль чрезвычайно важен, поскольку нарушение регуляции LypABC оказывается высокотоксичным для бактериальных клеток.
Подчёркивая пластичность бактериальных белковых доменов, данное исследование расширяет фундаментальные знания о механизмах переноса генов между бактериальными клетками и даёт важную подсказку для понимания того, как возникает антимикробная резистентность.
Первый автор исследования, д-р Эмма Бэнкс, стипендиат-исследователь Королевской комиссии Всемирной выставки 1851 года, отметила: «Особенно интересно то, что LypABC по своей структуре напоминает иммунную систему, и тем не менее бактерии используют её для высвобождения частиц GTA. Это наводит на мысль о том, что иммунные системы могут быть эволюционно перенастроены таким образом, чтобы помогать бактериям обмениваться ДНК друг с другом, — а это процесс, способствующий распространению устойчивости к антибиотикам».
Следующим шагом в исследовании станет выяснение того, как именно активируется управляющий узел LypABC и каким образом он обеспечивает разрыв бактериальных клеток и высвобождение частиц GTA.
Статья «Бактериальная CARD-NLR-подобная иммунная система контролирует высвобождение агентов переноса генов» опубликована в журнале Nature Microbiology.
Перевод статьи из ScienceDaily

Комментарий